 Forscher der New York University (NYU) haben ein 3D-gedrucktes Modell entwickelt, das die Bedingungen nachbildet, unter denen sich Krebszellen ausbreiten. Das in der Fachzeitschrift Life Science Alliance veröffentlichte Modell ermöglicht es Wissenschaftlern, den Metastase-Prozess zu untersuchen, der bislang schwer zugänglich war. Dies könnte neue Möglichkeiten zur Früherkennung und Behandlung von Krebs bieten, der das Risiko hat, sich im Körper zu verbreiten. Das Forschungspapier kann nachgelesen werden unter dem Titel „Direct visualization of emergent metastatic features within an ex vivo model of the tumor microenvironment„.
Forscher der New York University (NYU) haben ein 3D-gedrucktes Modell entwickelt, das die Bedingungen nachbildet, unter denen sich Krebszellen ausbreiten. Das in der Fachzeitschrift Life Science Alliance veröffentlichte Modell ermöglicht es Wissenschaftlern, den Metastase-Prozess zu untersuchen, der bislang schwer zugänglich war. Dies könnte neue Möglichkeiten zur Früherkennung und Behandlung von Krebs bieten, der das Risiko hat, sich im Körper zu verbreiten. Das Forschungspapier kann nachgelesen werden unter dem Titel „Direct visualization of emergent metastatic features within an ex vivo model of the tumor microenvironment„.
Dank Fortschritten in der Prävention, Diagnose und Behandlung haben viele Krebspatienten gute Heilungschancen. Allerdings breiten sich einige Tumore weiterhin auf andere Organe aus, was als Metastase bezeichnet wird. Metastasen sind besonders schwer zu behandeln und verantwortlich für die meisten Todesfälle bei Krebserkrankungen.
Carlos Carmona-Fontaine, Professor für Biologie an der NYU und Hauptautor der Studie, erklärt:
„Die Untersuchung des Moments, in dem eine weitgehend passive Tumorzelle die Fähigkeit zur Bewegung erlangt und metastasiert, könnte für die Krebsbehandlung entscheidend sein. Leider ist es nahezu unmöglich, diesen Übergang direkt zu beobachten, weshalb es derzeit keine Therapien gibt, die auf diesen wichtigen Schritt im Verlauf von Krebs abzielen.“
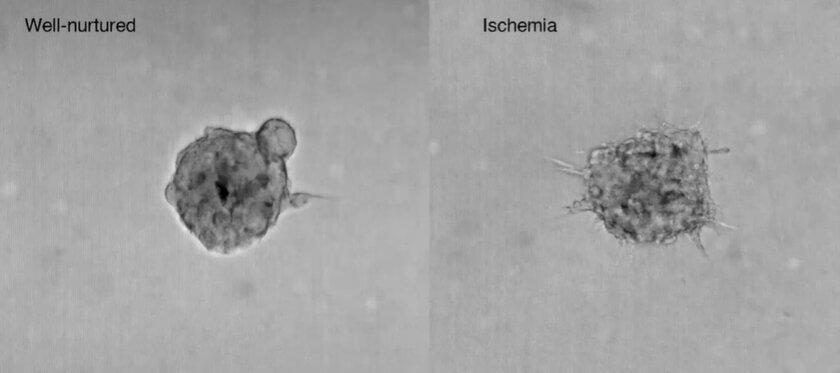
Die meisten metastasierenden Zellen entstehen in tiefen Gewebeschichten von Tumoren, in denen Sauerstoff und Nährstoffe knapp sind. Diese Ressourcenknappheit spielt eine entscheidende Rolle bei der Auslösung von Metastasen. Doch aufgrund der Lage der Zellen ist es schwierig, diesen Prozess in Patienten oder gängigen Labor-Modellen zu beobachten.
Miniaturisiertes Tumormodell „3MIC“ (3D-Mikroumgebungskammer)
Um dieses Problem zu lösen, entwickelten die Forscher ein miniaturisiertes Tumormodell, das die spezifischen Bedingungen simuliert, unter denen Tumorzellen metastasierende Eigenschaften entwickeln. Das Modell, das als „3MIC“ (3D-Mikroumgebungskammer) bezeichnet wird, erlaubt die Beobachtung von Tumorzellen in Echtzeit mithilfe von Mikroskopie. Mit Hilfe von 3D-Drucktechnologien gestalteten sie das Modell so, dass es eine detaillierte Bildgebung der tiefen und nährstoffarmen Zellen ermöglicht.
„Eine der wichtigsten Bedingungen für die Entstehung von Metastasen, der Mangel an Nährstoffen und Sauerstoff, war besonders schwer nachzubilden und vermutlich die größte Innovation des 3MIC“, sagte Carmona-Fontaine.
Das Modell ermöglichte es den Forschern auch, andere Zelltypen wie Makrophagen und Fibroblasten hinzuzufügen, die bekanntermaßen während der Metastasenbildung mit Tumorzellen interagieren. Dadurch konnten sie untersuchen, wie Tumorzellen unter verschiedenen Stoffwechselbedingungen wandern, eindringen und mit diesen anderen Zellen zusammenarbeiten.
Interessante Ergebnisse der Forscher
In ihrer Studie konnten die Forscher bestätigen, dass bekannte Faktoren, die Metastasen fördern, wie Sauerstoffmangel, auch in dem 3MIC-Modell eine Rolle spielen. Überraschenderweise zeigte ihre Untersuchung zudem, dass niedriger Sauerstoffgehalt den pH-Wert der Tumorumgebung senkt und diese saurer macht, was indirekt die Metastasenbildung fördert.
Darüber hinaus zeigten die Forscher, dass bestimmte Medikamente, wie Chemotherapievarianten des Wirkstoffs Taxol, die normalerweise gegen Tumorzellen wirken, in den ressourcenarmen Tumorzellen des 3MIC-Modells nicht anschlugen. Dies könnte darauf hindeuten, dass metastasierende Krebszellen aufgrund intrinsischer Veränderungen resistenter gegen Medikamente sind und nicht einfach aufgrund einer niedrigeren Wirkstoffkonzentration.
„Die Bedingungen, die wir im 3MIC beobachten, schaffen möglicherweise eine Umgebung, die Tumore vor bestimmten Behandlungen schützt, was erklären könnte, warum Metastasen so schwer zu behandeln sind“, fügte Carmona-Fontaine hinzu.
Mit dem 3MIC-Modell fokussieren sich die Forscher nun darauf, frühe Anzeichen der Metastasierung zu identifizieren, bevor sich die Zellen ausbreiten. Dies könnte als diagnostisches Werkzeug genutzt werden, um Metastasen vorherzusagen und potenzielle Therapieziele zu testen, die diesen Prozess unterbrechen könnten.